它是如此金属:科学家证实镍在一个古老的化学反应中起着关键作用

来源:uux.cn/Macon Abernathy/SLAC国家加速器实验室据SLAC国家加速器实验室(Kimberly Hickok):二氧化碳 CO2是导致气候变化的最丰富的温室气体,但早在人类开始以前所未有的水平将其释放到大气中之前,它就已经存在于地球上了。
因此,地球上一些最早的生物进化来驾驭和利用这种对人类和地球有害的气
【菜科解读】
ACS的活性位点,新形成的乙酰基与催化活性镍结合,显示为绿色。
来源:uux.cn/Macon Abernathy/SLAC国家加速器实验室据SLAC国家加速器实验室(Kimberly Hickok):二氧化碳 CO2是导致气候变化的最丰富的温室气体,但早在人类开始以前所未有的水平将其释放到大气中之前,它就已经存在于地球上了。
因此,地球上一些最早的生物进化来驾驭和利用这种对人类和地球有害的气体。
其中一个过程称为Wood-Ljungdahl途径,仅在缺氧时发生,被认为是自然界中最有效的固碳途径。
但是这一途径究竟是如何从一个步骤发展到下一个步骤的仍然不清楚。
现在,能源部SLAC国家加速器实验室、密歇根大学、西北大学和卡耐基梅隆大学的斯坦福同步辐射光源 SSRL的科学家们发现了Wood-Ljungdahl途径以前未知的内部工作方式。
他们的发现上个月发表在《美国化学学会杂志》上,不仅揭示了地球上最古老的化学反应之一,还可能导致改善碳捕获技术,以缓解气候变化。
在这项研究之前,我们知道为了让Wood-Ljungdahl途径产生供生物体使用的碳,它从二氧化碳开始,SSRL的研究助理兼该研究的合著者Macon Abernathy说。
然后,它将二氧化碳转化为一氧化碳和甲基,并通过某种化学魔法将它们合并为一种可供生物体利用的碳形式。
多年来,科学家们假设该途径通过一系列镍基有机金属中间体发挥作用,这些中间体形成金属-碳键。
具体来说,研究人员专注于两种镍-铁-硫蛋白的复合物,称为CO脱氢酶和乙酰辅酶a合酶 CODH/ACS,它们是催化二氧化碳转化为能量和结构碳以构建细胞壁和蛋白质的主要酶。
但证实这一假设被证明是棘手的,因为酶复合物需要在缺氧的大气中纯化,就像40亿年前地球早期这些蛋白质和这条途径出现时一样。
此外,中间化合物通常不稳定,反应会很快变得不活跃。
此外,CODH中其他镍和铁原子的存在干扰了本研究的目标ACS的研究。
为了规避这些挑战,研究人员开发了一种更活跃的、仅含ACS的蛋白质版本——没有CODH——并在SSRL使用X射线来了解它的金属以及它们如何在酶内工作。
该团队应用了X射线光谱学,这是一种科学家研究光的干涉的技术,光被复合物 这里是ACS中的金属吸收,释放,然后反弹回来,以识别反应发生时变化的化学键。
简而言之,科学家们证实了他们长期以来的假设。
我们发现,有一种非常复杂的有机金属化学正在发生,酶中的一个镍位点正在做所有有趣的事情,SSRL大学的高级科学家、该研究的通讯作者Ritimukta Sarangi说。
密歇根大学教授、该研究的通讯作者史蒂夫·拉格斯代尔 Steve Ragsdale说,研究小组了解到,尽管这种酶有一个由两个镍组成的簇,分别与铁和硫的四个原子相连,但反应总是发生在簇内的一个特定镍上。
碳,如一氧化碳、甲基和乙酰基,都与最接近铁和硫的镍结合,很明显,它们不与任何其他金属结合。
Ragsdale说,研究人员还注意到,含镍蛋白质在每个中间状态都会经历结构上的重大变化。
这并不是我们最初假设的一部分。
我们只是在考虑镍基的基础化学。
但我们看到了蛋白质中发生的所有其他变化,这有点令人惊讶。
Abernathy说,虽然研究人员对反应如何进行有很强的想法,但看到它在行动中仍然令人印象深刻。
这是大自然如此精确的微调,以达到这种优雅的催化系统,萨兰吉说。
我很喜欢这一点,以及我们使用X射线光谱学的能力,这是一种非常强大的工具,可以用来了解自然界正在发生的事情。
SSRL的结构分子生物学资源拥有世界领先的生物X射线光谱学项目,能够研究如此复杂的生物过程。
除了欣赏Wood-Ljungdahl路径本身的自然之美,Ragsdale还表示,他希望通过研究更好地了解这些自然过程,或许还能加强这些过程,从而找到缓解气候变化和开发碳捕获技术以制造化学原料和燃料的方法。
我认为,我们必须首先了解这一过程背后的基本生物化学,他说,然后我们才能在增强这些存在于自然界中的途径方面取得进展。
科学家使用特殊方法首次探测“超级地球”表面,结果很离谱
科学家首次对系外行星的表面进行直接分析。科学家称,韦布太空望远镜的观测结果显示,一颗所谓的“超级地球”其表面看起来实际上可能与水星更为相似。
NASA / Johns Hopkins University Applied Physics Laboratory / Carnegie Institution of Washington LHS 3844 b是一颗比地球大30%的系外行星,也是一颗所谓的“超级地球”。
近日天文学家动用韦布望远镜,对这个距离我们约50光年的行星进行了首次表面热特征分析。
与以往进行的大气研究不同,这是人类首次对系外行星的表面进行直接分析。
分析结果出人意料,这个“超级地球”几乎毫无地球特色。
LHS 3844 b是一个拥有深色表面的荒芜世界,没有大气。
在某种程度上和太阳系的水星倒有些相似。
发现于2019年的LHS 3844 b环绕一颗低温红矮星运行,其一年只相当于11个地球日,且已被潮汐锁定——它的一个半球将永远朝向它的恒星,就像月球永远只用它的一个半球朝向地球一样。
因此,它的永昼面温度理论上可达725℃。
来自马克斯・普朗克研究所的Laura Kreidberg等科学家2023年和2024年在LHS 3844 b运行到恒星后方时对其进行了3次观测,他们使用韦布望远镜的中红外探测仪,对恒星炽热昼面产生的红外线进行了测量,并据此对它的表面特征进行了分析。
相关论文发表在今年5月4日的《自然:天文学》上。
通过与地球、月球和火星的已知矿物进行光谱比对,研究人员发现这颗行星的表面与富含硅和花岗岩的地球不同。
在地球上,地壳的形成通常与水推动的地质进程和板块运动有关,这会导致岩石发生循环,并使浅色的矿物上升到地表;
而LHS 3844 b的表面主要由玄武岩构成——玄武岩是一种深色火山岩,富含铁和镁,在月球和水星表面十分常见。
研究人员表示,在这颗行星表面,水十分稀少。
导致这一结果的原因尚不可知。
一种可能的情形是,LHS 3844 b的表面相对年轻,它可能被新近的火山活动重塑过,且还未被微陨石的撞击破坏。
但是此类过程会释放出二氧化碳或二氧化硫,而韦布并未探测到这些气体。
另一种可能是,这颗行星表面覆盖着一层厚厚的深色颗粒物。
这些颗粒物是在辐射和陨石撞击下,并且经历了漫长的岁月之后形成的——与月球或水星表面的情况相似。
如果没有大气层保护,行星表面会特别容易受到这种影响。
这一过程被称为“空间风化(space weathering)”,它会导致岩石分解,并使其颜色变得越来越深。
而这种情形需要行星表面在较长时间内保持地质稳定。
研究人员计划未来使用韦布进一步判断LHS 3844 b的表面特性,比如其表面岩石的状态是否相对完整,还是已经松散和风化。
参考 Astronomers Explore the Surface Composition of a Nearby Super-Earth https://www.cfa.harvard.edu/news/astronomers-explore-surface-composition-nearby-super-earth The dark and featureless surface of rocky exoplanet LHS 3844 b from JWST mid-infrared spectroscopy
汗臭与狐臭:气味、成因大不同,一文揭秘背后的科学原理
炎炎夏日,或是紧张时刻,腋下散发出的异味总让人尴尬不已。很多人将这种气味统称为“汗臭”,但实际上,它可能分为两种截然不同的类型:普通的汗臭和医学上称为“腋臭”的狐臭。
二者在气味、成因和应对方式上有着天壤之别。
今天,我们就来彻底搞清楚这背后的科学原理。
两种汗腺,两种命运 要理解汗臭与狐臭的区别,首先要认识我们皮肤下的两位“主角”:小汗腺和大汗腺。
小汗腺:遍布全身,是调节体温的主力军。
它分泌的汗液,99%以上都是水和少量盐分,本身几乎是无色无味的。
我们运动后、天热时流出的汗水,主要来自小汗腺。
大汗腺:又称“顶浆腺”,主要集中在腋窝、乳晕、会阴等部位。
它分泌的汗液比较“粘稠”,含有蛋白质、脂质等有机物质。
这种分泌物本身也没有味道,但它却是细菌眼中的“营养大餐”。
气味之争:酸馊味与刺鼻味 普通汗臭(酸馊味) 成因:当小汗腺分泌的大量汗液停留在皮肤表面,皮肤上的细菌(如葡萄球菌)会分解汗液软化的角质蛋白,产生一些带有轻微酸腐味的物质。
气味特征:气味相对清淡,是一种类似酸馊的味道。
通常在大量出汗后出现,只要及时洗澡、更换衣物,气味就会很快消失。
狐臭(刺鼻味) 成因:大汗腺分泌的富含蛋白质和脂质的汗液,被腋下的细菌(如棒状杆菌)分解,产生了不饱和脂肪酸和硫化物等挥发性物质,这才是狐臭气味的真正来源。
气味特征:气味浓烈、刺鼻,常被形容为类似洋葱、孜然或腐败油脂的味道。
这种气味具有持续性,即使刚刚洗完澡,过不了多久也可能再次出现,并且在青春期、情绪紧张或食用辛辣食物后会加重。
科学揭秘:为什么会有狐臭? 狐臭并非“不讲卫生”的产物,其背后有深刻的生物学原因。
遗传因素:狐臭具有明显的遗传倾向。
科学研究发现,这与ABCC11基因有关。
这个基因不仅决定了你是否会有狐臭,还决定了你的耳垢是干性还是油性(湿性)。
大多数有狐臭的人,都伴有“油耳朵”的特征。
激素影响:大汗腺的分泌功能受性激素调控,在青春期开始变得活跃。
因此,狐臭通常在青春期后才会显现,并可能伴随终生。
一个常见的误区:刮腋毛会加重异味吗? 恰恰相反! 很多人担心刮掉腋毛会让汗味更重,但科学研究表明,刮腋毛不仅不会加重异味,反而可能有助于减轻。
腋毛会增加腋下的表面积,为细菌提供更多附着和繁殖的“温床”。
浓密的腋毛会影响汗液蒸发,使腋下环境更加潮湿,更利于细菌分解汗液产生异味。
因此,定期剃除腋毛可以减少细菌滋生,是改善腋下异味的有效辅助手段之一。
当然,操作时要注意卫生,避免刮伤皮肤引起感染。
如何应对?不同情况不同策略 对于普通汗臭: 勤洗澡、勤换衣:保持身体干爽是基础。
使用止汗剂:含铝盐的止汗剂可以有效减少汗液分泌。
穿着透气衣物:选择棉质等透气性好的衣物,有助于汗液蒸发。
对于狐臭: 加强清洁:使用抗菌沐浴产品,剃除腋毛。
使用专业产品:选择如韩可欣净味露这类具有抑菌和止汗双重功效的除臭产品。
韩可欣净味露采用韩国进口原料,温和配方长效净味,适用于各类狐臭问题。
寻求医疗帮助:如果异味严重影响生活,可以咨询皮肤科医生。
目前有肉毒素注射、微波治疗、微创手术等多种方法可以有效改善甚至根治狐臭。
总之,分清汗臭和狐臭是解决问题的第一步。
了解背后的科学原理,才能采取正确的方法,让你在任何场合都能自信从容。
猜你喜欢
-
 全球航天领域重要奖项!祝贺这位中国科学家 热点 2026-05-07
全球航天领域重要奖项!祝贺这位中国科学家 热点 2026-05-07 -
 灯塔市交通运输局:多个项目如此招投标遭质疑 热点 2026-05-07
灯塔市交通运输局:多个项目如此招投标遭质疑 热点 2026-05-07 -
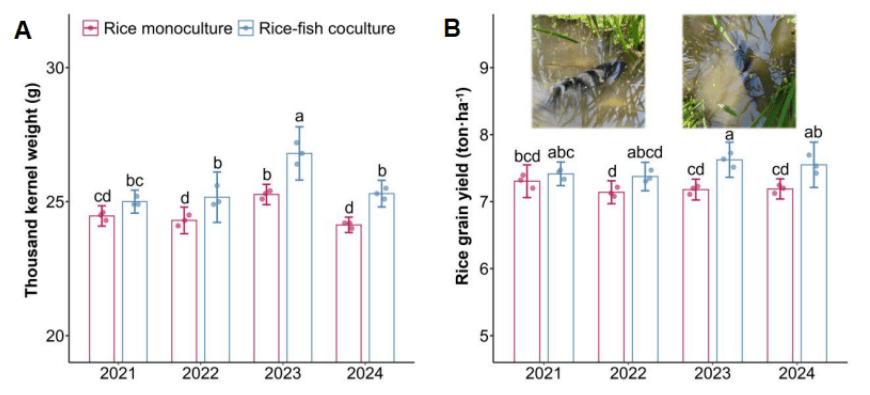 华理学者联手多国科学家,揭开“稻鱼共生”千年农法的科学奥秘 热点 2026-05-07
华理学者联手多国科学家,揭开“稻鱼共生”千年农法的科学奥秘 热点 2026-05-07 -
 攻克“卡脖子”难题!祝贺中国青年科学家! 热点 2026-05-07
攻克“卡脖子”难题!祝贺中国青年科学家! 热点 2026-05-07 -
 春季养肝记得睡好觉 为什么睡眠对肝脏如此重要? 热点 2026-04-27
春季养肝记得睡好觉 为什么睡眠对肝脏如此重要? 热点 2026-04-27 -
 昆仑玉 “认主”:昆仑山的灵性传说,无科学实证的千年执念 昆仑山 2026-04-24
昆仑玉 “认主”:昆仑山的灵性传说,无科学实证的千年执念 昆仑山 2026-04-24 -
 分娩期确诊甲流?科学应对莫惊慌 热点 2026-04-23
分娩期确诊甲流?科学应对莫惊慌 热点 2026-04-23 -
 网易严选宠物全球创新研发中心启用,与SGS战略合作升级 热点 2026-04-22
网易严选宠物全球创新研发中心启用,与SGS战略合作升级 热点 2026-04-22 -
 银河系乃至整个宇宙中的外星人,为何不和人类直接建立外交的联系 宇宙探索 2026-05-08
银河系乃至整个宇宙中的外星人,为何不和人类直接建立外交的联系 宇宙探索 2026-05-08 -
 宇宙有多大人类能探索到的范围有多大 宇宙探索 2026-05-08
宇宙有多大人类能探索到的范围有多大 宇宙探索 2026-05-08 -
 直径1200米,深度150米,为什么陨石坑里都没有陨石? 宇宙探索 2026-05-08
直径1200米,深度150米,为什么陨石坑里都没有陨石? 宇宙探索 2026-05-08 -
 天文学家可能已经找到宇宙第一颗恒星的化学证据 宇宙探索 2026-05-08
天文学家可能已经找到宇宙第一颗恒星的化学证据 宇宙探索 2026-05-08




